Seit Ende 2019 ist die gesamte Welt mit dem Coronavirus beschäftigt. Die Pandemie hat sich stark ausgebreitet und bisher zu rund 20.6 Mio. bestätigten Infektionen und über 750’000 Todesfällen geführt. Die Pharmaindustrie arbeitet auf Hochtouren, um den Virus mit Medikamenten zu bekämpfen und mit einem Impfstoff die Menschen vor einer Infektion schützen zu können.
Mögliche Medikamente
Ein längerfristiger Schutz und ein Eindämmen der Pandemie ist vermutlich lediglich über ein Vakzin möglich. Da aber eine Entwicklung eines Impfstoffs selbst in Ausnahmesituationen gewisse klinische Studien durchlaufen muss und nicht sofort verfügbar ist, müssen Medikamente die Krankheitsverläufe bis dahin unter Kontrolle bringen. Viren sind kleine infektiöse Partikel. Sie betreiben selbst keinen Stoffwechsel, sondern brauchen die Hilfe von anderen Zellen, um sich vermehren zu können. Das bedeutet, Viren schleichen sich in Zellen eines Menschen oder eines Tiers ein, manipulieren die zelleigene Reproduktionsfabrik und können sich so ausbreiten. Um diesen Vorgang zu stoppen, setzt die Forschung auf die folgenden Methoden:
1) Antivirale Medikamente:
Darunter versteht man Präparate, die verhindern, dass Viren RNA oder DNA-Stränge von der Wirtszelle kopiert und somit die Viren vermehrt werden. Ebenfalls können sie das Verlassen von neuen Viren aus der Wirtszelle verhindern.
2) Immun-Suppressive:
Darunter fallen Medikamente, welche die überstarke Immunreaktion im Körper kontrollieren und so verhindern, dass der Körper sich selber durch eine starke innere Entzündung schwächt.
3) Antikörper
Darunter versteht man Medikamente, die künstliche oder menschliche Antikörper (von genesenen Patienten) enthalten und so die Viren an der Fusion mit den menschlichen Wirtszellen hindern können.
Unter den vielen Forschungsinitiativen ist vor allem Remdesivir von Gilead (ein antivirales Medikament), dem ersten Medikament gegen SARS-CoV‑2 mit einer Notfallzulassung in den USA und Europa, bekannt.
Verschiedene Impfstoffe in der Entwicklung
Medikamente alleine werden aber nicht ausreichen, um die Pandemie zu beenden. Dafür braucht die Mehrheit der Bevölkerung eine Immunabwehr, die nur über eine langwierige Durchseuchung oder über die Verabreichung eines Impfstoffes erreicht werden kann. Per Ende Juli 2020 befinden sich über 20 Impfstoff-Kandidaten in klinischen Studien. Das heisst, die möglichen Impfstoffe werden bereits an Menschen getestet. Insgesamt kann man die Impfstoff-Technologien in vier Gruppen unterteilen:
1) Lebend-Impfstoffe:
Diese bestehen aus lebenden, aber geschwächten Versionen des Virus. Sie sind immer noch in der Lage, die Zellen unseres Körpers zu infizieren und eine Immunantwort auszulösen, aber zu schwach, um schwere Krankheiten zu verursachen. Die Produktion dieser Art ist aufwändig, da die Viren in Kulturen heranwachsen müssen. Daher ist diese Technologie praktisch kein Thema im Kampf gegen Covid-19.
2) Inaktivierte / Tot-Impfstoffe
Diese werden aus abgetöteten Versionen, respektive Teilen der Zellwand des Virus gewonnen. Solche Teilchen werden von unseren Immunzellen erkannt, können aber keine Krankheiten verursachen. Auch hier braucht es eher aufwändige Verfahren, um grosse Mengen herstellen zu können. In China, wo man bereits früh mit dem Virus in Kontakt kam, gibt es aber Impfstoffe dieser Art, welche fortgeschritten sind. Neben den beiden chinesischen Firmen Sinovac Biotech sowie Sinopharm ist aber auch das Projekt von Sanofi mit Glaxo Smithkline oder Novovax mit dieser Technologie unterwegs. Während die beiden chinesischen Unternehmen bereits Phase 1 und 2 abschliessen konnten und die finale 3. Phase erreicht haben, befindet sich Sanofi noch in einer frühen Entwicklungsstufe. Jedoch ist deren Technologie bereits für zugelassene Impfstoffe verwendet worden und hat daher viel Potenzial.
3) Vektor-Impfstoffe
Diese bestehen aus harmlosen Viren (Erkältungsviren wie das Adenovirus), die so modifiziert wurden, dass sie Antigene des Zielerregers enthalten. Die modifizierten Viren fungieren als Trägersysteme, die die Antigene unseren Immunzellen anzeigen. Die Produktionstechnologie ist nicht trivial, aber bereits etabliert und in der Lage grosse Mengen zu produzieren. Damit ist dies eine der hoffnungsvollsten Technologien im Kampf gegen Covid-19. Insbesondere Johnson&Johnson, die Oxford Universität zusammen mit AstraZeneca, Merck & Co. oder CanSino aus China sind in dieser Technologie tätig. Johnsons&Johnson verfügt über grosses Know-how, hat aber erst im Juli die Phase 1 gestartet. Auch Merck & Co. ist sehr spät in das Rennen eingestiegen und steckt noch in präklinischer Entwicklung. Jedoch ist deren Technologie bereits für eine Ebola-Impfung 2019 eingesetzt worden. Weitere Kandidaten sind AstraZeneca zusammen mit Oxford, welche schon in finaler Phase 3 testen und als Spitzenreiter gelten. Auch CanSino aus China startete im Juli eine finale Phase 3 Studie.
4) Gen-basierte Impfstoffe
Diese Gruppe umfasst Impfstoffe, die aus “Boten-RNA” bezeichneten Molekülen (mRNA) oder DNA-Sequenzen bestehen. Diese kodieren Teile des Zielerregers.In den Zellen unseres Körpers werden die RNA- oder DNA-Moleküle in Antigene umgewandelt, die dann von unseren Immunzellen erkannt werden. Diese Technologie ist hoch effizient und einfach in der Produktion. Es handelt sich um ein chemisch-enzymatisches Verfahren, welches sehr schnell auf den Markt kommen kann. Jedoch ist die Technologie neu und es gibt noch kein Produkt am Markt. Neben Moderna sind auch BioNtech/Pfizer, CureVac oder Inovio mit dieser neuartigen Technologie unterwegs. Moderna war die erste Firma, welche den Gencode von SARS-CoV‑2 in kurzer Zeit in einen Kandidaten formulieren konnte. Im Juli wurde eine finale Phase 3 Studie gestartet. Auch BioNtech zusammen mit Pfizer haben eine Phase 2/3 gestartet und wollen noch im Herbst neue, finale Daten publizieren. Deren Entwicklung beinhaltet sogar vier verschiedene RNA-Kandidaten, was die Chancen erhöht. CureVac sowie auch Inovio befinden sich noch in Phase 1 und haben etwas Rückstand auf die beiden Konkurrenten.
Drei Kandidaten haben Studiendaten zur Phase 1 publiziert
Im Juli haben die drei führenden Unternehmen Moderna, AstraZeneca/Oxford sowie BioNtech/Pfizer allesamt Studiendaten zu ihrer Phase 1 Studie publiziert. Auch wenn die Studien in einer Phase 1 relativ klein sind und daher nur wenige Freiwillige fassen, geben die Resultate Hoffnung. Alle Kandidaten haben im menschlichen Körper die Produktion von neutralisierenden Antikörpern angeregt, wobei die Menge mindestens so hoch war wie bei genesenen Patienten. Noch wichtiger ist, dass alle Kandidaten auch die Bildung von T‑Zellen für die Bekämpfung von Viren angeregt haben, wobei es da bei den verschiedenen Impfstoffen Unterschiede gab. Ebenfalls traten lediglich kleinere Nebenwirkungen wie Kopfschmerzen, Müdigkeit oder Hautrötungen auf. Vereinzelt wurden bei höherer Dosierung auch kurzfristige Fieberschübe festgestellt. Es waren jedoch keine grösseren, anhaltenden Nebenwirkungen zu beobachten. Obschon die Resultate vielversprechend sind, müssen grössere Studien abgewartet werden, welche die Verhinderung einer Covid-Erkrankung testen. Alle drei Unternehmen befinden sich mit ihren Impfkandidaten nun in der wegweisenden Phase 3‑Studie mit jeweils rund 30’000 Probanden.
Auftragsproduzenten spielen eine wichtige Rolle
In der Regel dauert die gesamte Entwicklung eines Impfstoffes zwischen 8 und 15 Jahre. So viel Zeit ist aktuell aber nicht vorhanden. Der Zeitplan wurde enorm gekürzt. Viele Studien werden parallel durchgeführt. Ebenfalls wurden bereits mit Tests an Menschen begonnen, bevor überhaupt Daten von Tiermodellen zur Verfügung standen. Dies ist nur in Ausnahmesituationen denkbar. Es ist enorm erstaunlich und positiv, wie schnell die Pharmaindustrie vorankommt. Um aber bei diesem Tempo auch die nötigen Produktionskapazitäten bereitstellen zu können, kommen Auftragsproduzenten, sogenannte CDMO’s (Contract Development & Manufacturing Organizations) ins Spiel. Viele grosse Pharmakonzerne, aber vor allem auch kleine Biotech-Firmen können oder wollen die Risiken des Kapazitätsausbaus während der klinischen Studien nicht tragen. Beim Verfehlen der Ziele eines Medikamentes würden bis zu mehreren 100 Mio. Franken verloren gehen. Das Auslagern dieser Kapazitäten an Auftragsproduzenten ist daher sehr populär geworden. Durch Covid-19 könnte sich dieser Prozess sogar noch beschleunigen. Dafür gibt es drei Gründe:
1) Unterbrochene Lieferketten
Covid-19 hat gezeigt, dass viele Regionen von der Wirkstoff-Produktion asiatischer Länder abhängig sind. Viele einfache chemische Wirkstoffe wurden in den letzten Jahrzehnten in günstige Produktionsländer ausgelagert – fehlen aber nun teilweise, weil Lieferketten unterbrochen sind. Dies wird dazu führen, dass vermehrt wieder lokaler produziert wird.
2) Hohe Kapazitäten
Falls Covid-19 ohne Impfstoff nicht verschwinden wird, führt dies zwangsweise dazu, dass ein sehr grosser Anteil der Bevölkerung geimpft werden muss. Bis 2019 haben die vier Marktführer Glaxo Smithkline, Merck & Co, Sanofi und Pfizer insgesamt pro Jahr knapp 3 Mrd. Dosen an verschiedenen Impfstoffen produziert. Gegen Covid-19 könnten aber noch viele weitere Milliarden Dosen benötigt werden. Diese Grössenordnung kann nur über Kooperationen mit grossen CDMOs bereitgestellt werden.
3) Aufrüsten für die Zukunft
Einige Pharmakonzerne werden sich die zukünftige Auslagerung genau überlegen, um selber für spezielle Fälle mehr Kapazitäten generieren zu können.
Der bisher am weitesten fortgeschrittene Impfstoff-Hersteller Moderna hat mit Lonza einen 10-Jahres Vertrag abgeschlossen. Noch im Sommer 2020 soll der Wissenstransfer der neuen mRNA-Technologie sichergestellt werden, um am US-Standort von Lonza sowie in Visp pro Jahr mindestens 500 Mio. Dosen des Impfstoffes mRNA-1273 herstellen zu können. Lonza verfügt über die technischen Voraussetzungen sowie die Fähigkeit solche Projekte in kurzer Zeit auf höchster Qualität umzusetzen. Johnson&Johnson, welche bereits über ein grosses Know-how in der Herstellung von viralen Vektoren haben, zielen ebenfalls auf 1,5 Mrd. Dosen pro Jahr ab. Dafür wurden mit Catalent und Emergent BioSolutions Produktionsverträge ausgearbeitet. AstraZeneca, welche mit Oxford zusammenarbeitet, hat global eine Vielzahl von Partnerschaften aufgegleist, um jährlich bis zu 2 Mrd. Dosen herzustellen. Sanofi und Glaxo Smithkline wollen ebenfalls 1 Mrd. Dosen pro Jahr erreichen. Pfizer und BioNtech zielen ab 2021 sogar auf 1,3 Mrd. ab. Über Kooperationen ist bei beiden Kandidaten noch wenig bekannt. Alle bereits publizierten Ziel-Volumen summieren sich pro Jahr auf fast 8 Mrd. Dosen. Ob diese am Ende wirklich benötigt werden, bleibt abzuwarten.
Wann könnte ein erster Impfstoff verfügbar sein?
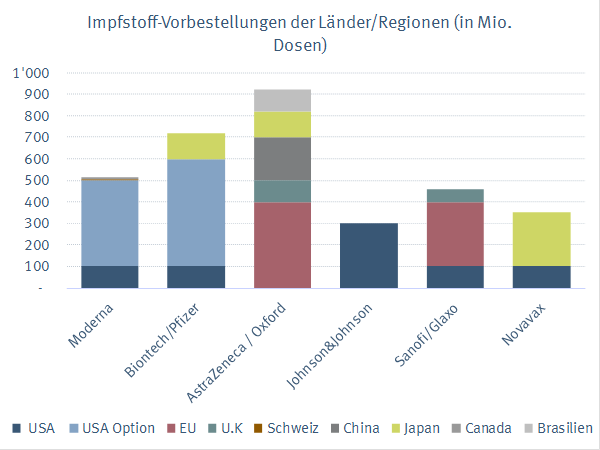
Dank globaler Kooperationen und staatlicher Programme (Warp Speed in den USA oder Inclusive Vaccine Alliance in Europa) werden hoffnungsvolle Projekte vorangetrieben. Ebenso unterstützen andere staatliche Organisationen die Prozesse oder helfen gar bei der Koordination von Studien mit. Auch die Regulierungsbehörden sind sich bewusst, dass beschleunigte Zulassungsverfahren notwendig sind, ohne dabei die Sicherheitsaspekte zu vergessen. Während globale Impfstoff-Allianzen meist das Ziel einer fairen Verteilung haben, zielen staatliche Gelder eher auf die Sicherung von zukünftigen Impfdosen ab, um damit die lokale Wirtschaft zu sichern. Bereits sind einige namhafte Versprechungen und Vorbestellungen gemacht worden. U.K hat sich 60 Mio. Dosen von Sanofi / Glaxo Smithkline für USD 625 Mio. (USD 12.50 pro Dose) sowie 100 Mio. Dosen von AstraZeneca/Oxford für einen unbestimmten Preis gesichert. Auch Brasilien hat sich schon 100 Mio. Dosen von AstraZeneca für USD 127 Mio. zusagen lassen (USD 4.20 pro Dose). Der grösste Deal ist aber bisher BioNtech/Pfizer gelungen. Die USA sichern sich vorerst 100 Mio. Dosen für USD 1.95 Mrd. (USD 19.5 pro Dose). Zudem haben sie eine weitere Option für 500 Mio. Dosen gesichert, falls nötig. Auch von Johnson&Johnson sichert sich die USA bis zu 300 Mio. Dosen. Hier werden für die ersten 100 Mio. Dosen USD 1 Mrd. fällig (USD 10 pro Dose). Von Sanofi/Glaxo sichert sich die USA 100 Mio. Dosen für USD 2.1 Mrd. (USD 21 pro Dose) und von Moderna letztlich 500 Mio., wobei für die ersten 100 Mio. Dosen USD 1.5 Mrd. gezahlt werden (USD 15 pro Dose). Japan hat ebenfalls schon 120 Mio. Dosen von AstraZeneca sowie 120 Mio. von Biontech/Pfizer für einen unbestimmten Preis gesichert. Während China bisher die Versorgung mit lokalen Playern bereitstellen möchte, hat die EU ebenfalls schon ordentlich zugeschlagen. Bereits 400 Mio. Dosen AstraZeneca sowie weitere 300 Mio. von Sanofi/Glaxo wurden gesichert. Auch die Schweiz ist in den Versorgungskampf eingestiegen. Nicht verwunderlich wurde der Vertrag mit Moderna unterzeichnet, welche ihren 2. Standort dank der Lonza-Kooperation nach Basel verlegen werden. Die Schweiz sichert sich 4.5 Mio. Dosen vom bisher teuersten Impfstoff, welcher über USD 30 pro Dose kosten könnte. Damit wird rund die Hälfte des jährlichen Schweizer Impfbudgets für den Kampf gegen das Virus eingesetzt. Ein zweiter Deal könnte mit Johnson&Johnson abgeschlossen werden, welche den Impfstoff durch ihre Tochter Janssen Vaccines in Bern produzieren werden.
AstraZeneca hat als erste Firma bereits mit einer Phase 2/3 Studie in England mit 10’260 Probanden begonnen. Erste Daten dazu werden im September publiziert. In diesen Studien geht es in erster Linie um eine Erweiterung der Altersstrukturen. Es werden neben Kindern auch ältere Erwachsene eingeschlossen, um die Wirkung des Impfkandidaten zu überprüfen.
Moderna startete im Juli mit einer Phase 3 Studie mit 30’000 Teilnehmern. Bereits im Oktober und dann im November sollen wegweisende Daten publiziert werden. Nebenbei läuft weiterhin eine Phase 2 Studie, welche im Juni begonnen wurde. Auch dabei geht es um die Überprüfung der Wirksamkeit bei Personen unter 55 und über 55 Jahren.
Auch BioNtech/Pfizer haben im Juli eine Phase 2/3 gestartet, welche um die 30’000 Probanden umfasst. Auch hier darf mit ersten Resultaten ab Oktober gerechnet werden.
Nicht ganz zu vergessen sind Sinovac und Sinopharm, welche ebenfalls in Phase 3 Studien stehen und noch 2020 eine Zulassung anstreben. Wir gehen bei den westlichen Projekten, welche globales Potential haben, davon aus, dass bei robusten Resultaten der Phase 3 ein Zulassungsantrag sogar noch 2020 formuliert werden kann und einer der Impfstoffe bereits eine Notfall-Zulassung erhalten könnte. Mit den laufenden Entwicklungsarbeiten und Fortschritten sind wir positiv gestimmt und erwarten, dass 2021 die ersten Personen geimpft werden können. Spätestens 2022 sollten dank grossen Kooperationen mit Auftragsproduzenten genügen Dosen für eine breite Impfung der Bevölkerung bereitstehen.
Disclaimer:
Die Informationen und Ansichten in diesem Blog dienen ausschliesslich Informationszwecken und stellen insbesondere keine Werbung, Empfehlung, Finanzanalyse oder sonstige Beratung dar. Namentlich ist dieser weder dazu bestimmt, dem Leser eine Anlageberatung zukommen zu lassen, noch ihn bei allfälligen Investitionen oder sonstigen Transaktionen zu unterstützen. Entscheide, welche aufgrund der vorliegenden Publikation getroffen werden, erfolgen im alleinigen Risiko des Anlegers.
Bei Fragen zu diesem Thema stehen wir Ihnen gerne zur Verfügung.
notablog@rahnbodmer.ch
Weitere Beiträge von Rahn+Bodmer Co.